Każdy z nas obawia się zachorowania na nowotwór złośliwy, dlatego poszukujemy wiedzy nt. możliwych objawów choroby nowotworowej. Jakie nowotwory najczęściej występują w Polsce u kobiet i mężczyzn, jakie czynniki mogą sprzyjać rozwojowi choroby? Zachęcamy do lektury tekstu.
Spis treści:
- Jakie nowotwory występują u kobiet i mężczyzn? Zachorowalność na nowotwory a śmiertelność z powodu nowotworów
- Nowotwory a wiek
- Objawy nowotworu
- Czynniki rakotwórcze – kancerogenne. Co sprzyja powstawaniu nowotworów?
- Podsumowanie
Jakie nowotwory występują u kobiet i mężczyzn? Zachorowalność na nowotwory a śmiertelność z powodu nowotworów
Zachorowalność na nowotwory w Polsce różni się w zależności od płci.
Mężczyźni – na jakie nowotwory w Polsce najczęściej chorują i z powodu jakich nowotworów najczęściej umierają?
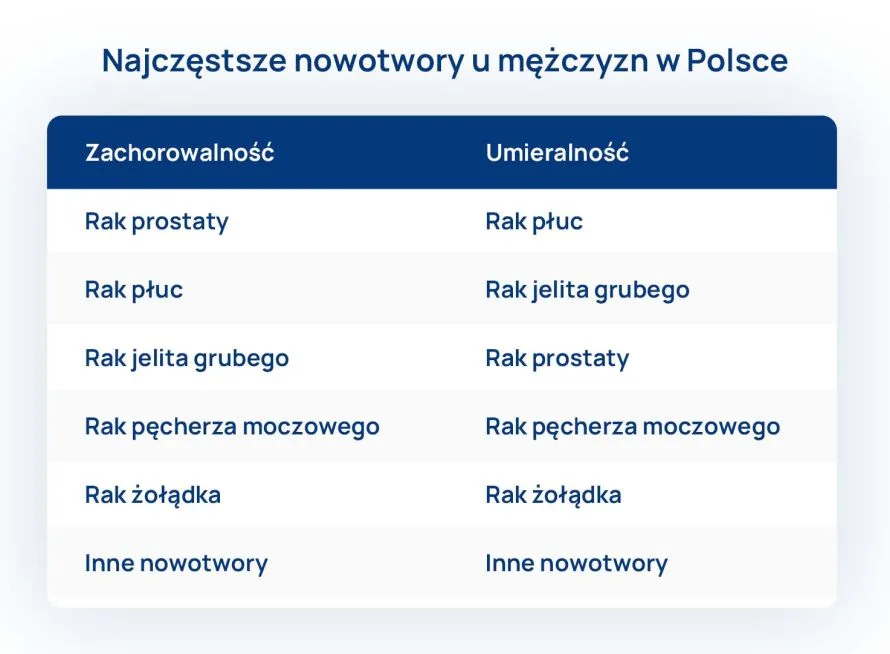
Dominującą przyczyną zgonów z powodu nowotworów u mężczyzn pozostaje rak płuc, chociaż od kilkunastu lat spada zachorowalność na ten nowotwór, co wiąże się ze zmniejszeniem odsetka palaczy tytoniu wśród płci męskiej w ciągu ostatnich kilku dekad.
>> To może Cię zainteresować: Rak żołądka – przyczyny, objawy, diagnostyka, leczenie

Kobiety – jaki jest najczęstszy rak u kobiet? Z powodu jakich nowotworów kobiety umierają najczęściej?
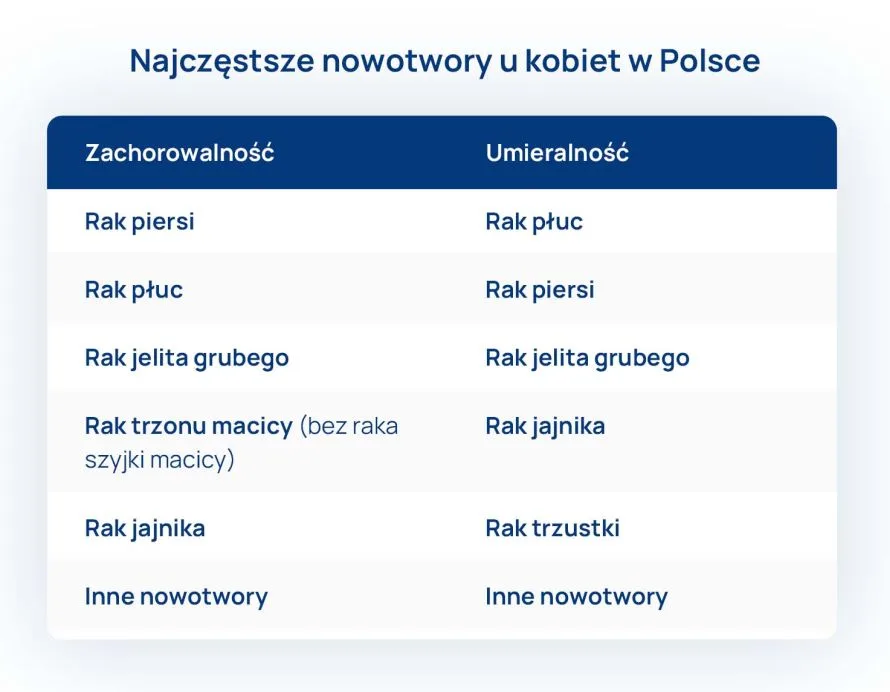
Najczęstszym nowotworem u kobiet jest rak piersi, jednak pierwszą przyczyną zgonów spowodowanych nowotworem wśród kobiet również jest rak płuc. Umieralność z powodu raka piersi została zahamowana w połowie lat dziewięćdziesiątych XX w, a na początku XXI w. zanotowano spadek liczby zgonów z tego powodu. Dzieje się tak dlatego, iż nowotwory piersi u kobiet są coraz lepiej leczone. Niestety kobiety zaczęły palić więcej tytoniu, dlatego rak płuc staje się u nich główną przyczyną śmierci spowodowanej nowotworem.
W populacji polskich kobiet rak trzustki ma mniejszą częstość występowania w porównaniu z innymi nowotworami. Niestety niski wskaźnik przeżywalności i późna wykrywalność plasuje go w czołówce nowotworów, które są przyczyną śmierci kobiet w Polsce.
>> Przeczytaj też: Rak jelita grubego – jakie są wczesne objawy?

Nowotwory a wiek
Częstość występowania nowotworów rośnie z wiekiem. W całej Polsce na nowotwór choruje rocznie ok. 1 tys. dzieci i ok. 60 tys. osób po 65 r.ż.
Trochę inna jest również struktura zachorowalności i śmiertelności z powodu raka w różnych grupach wiekowych.
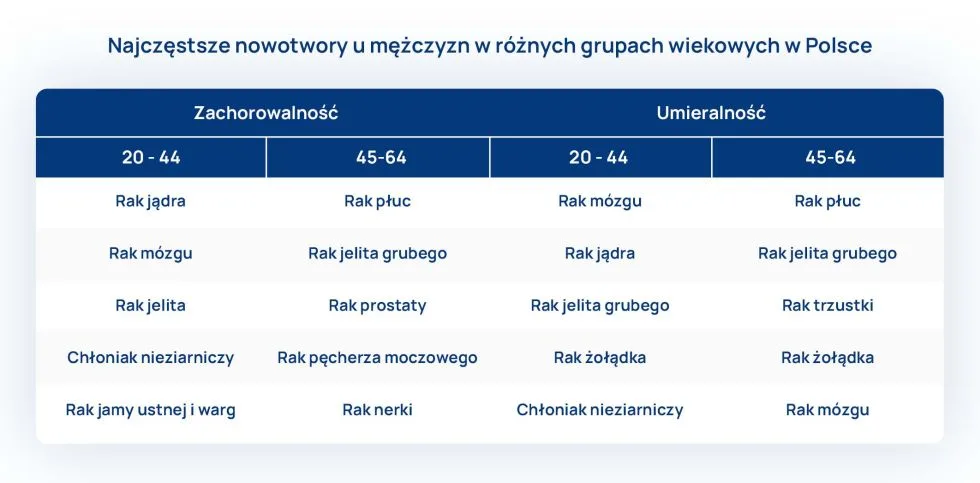
Najczęstsze nowotwory u mężczyzn w Polsce w zależności od wieku
U młodych mężczyzn (20-44 r.ż.) ważną rolę odgrywają nowotwory jąder, chłoniak nieziarniczy (non-Hodgkin lymphoma – NHL), nowotwory jamy ustnej (powodowane zakażeniem HPV) oraz rak mózgu. Do 65 r.ż znaczenia nabierają również nowotwory trzustki.
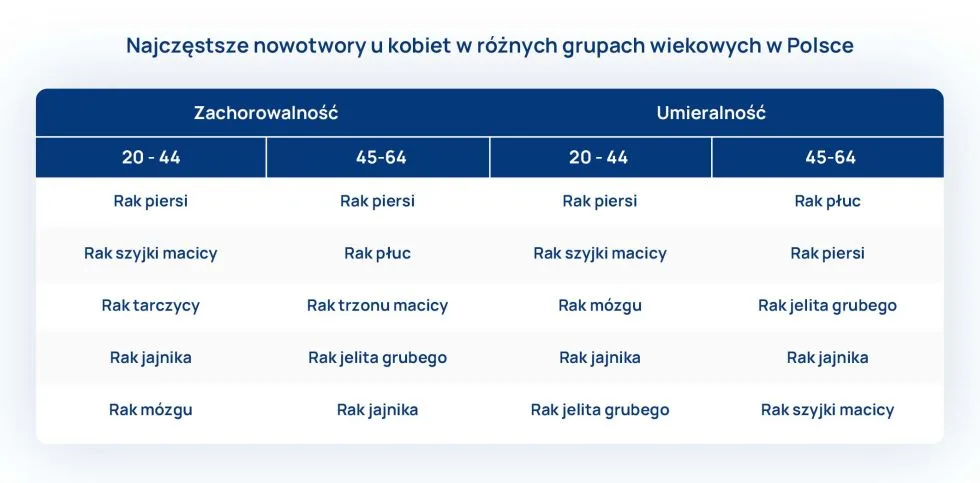
Najczęstsze nowotwory u kobiet w Polsce w zależności od wieku
U młodych kobiet (20-44 r.ż.) notuje się dużą zachorowalność na raka szyjki macicy, raka tarczycy oraz rak mózgu. W grupie kobiet do 65 r.ż śmiertelne żniwo zbiera rak szyjki macicy, pomimo, że nie występuje w grupie najczęstszych nowotworów tej grupy wiekowej.
>> Sprawdź także: Rak jajnika – objawy, czynniki ryzyka, diagnostyka laboratoryjna
Objawy nowotworu
Choroba nowotworowa zazwyczaj rozwija się przez lata, a jej objawy nie są widoczne. Obecność nowotworu w organizmie można zauważyć dopiero wówczas, gdy:
- komórki nowotworowe wydzielają w większych ilościach aktywną biologicznie substancję (cytokinę zapalną lub hormon);
- ognisko nowotworu powoduje ucisk na jakąś strukturę, powodując zablokowanie przewodu (np. przewodu żółciowego, a w efekcie żółtaczkę) lub naruszając ciągłość tkanek wewnętrznych lub zewnętrznych;
- znacząca liczba komórek nowotworowych ulega martwicy wywołując reakcję zapalną w organizmie;
- ognisko nowotworu, guz, rozwija się w miejscu widocznym lub oglądanym w celach profilaktycznych.
Niestety takie objawy nowotworu często wykrywa się w późnym stadium choroby nowotworowej, dlatego tak ważna jest profilaktyka raka, w tym wykonywanie badań profilaktycznych.
Czynniki rakotwórcze – kancerogenne. Co sprzyja powstawaniu nowotworów?
Ok. 80-90 % nowotworów złośliwych wiąże się z:
- niewłaściwym stylem życia – w tym brakiem aktywności fizycznej i złymi nawykami żywieniowymi;
- miejscem pracy i narażeniem na działanie czynników kancerogennych;
- miejscem zamieszkania;
- zachowaniami społeczno-kulturalnymi.
| Nowotwory złośliwe określane są jako „man made diseases” – czyli schorzenia wywoływane przez człowieka. |
Palenie tytoniu a nowotwory
Szacuje się, iż około 50% zgonów z powodu nowotworów ma związek z nowotworami, w tym
- 30% ma pewny i udowodniony związek z tym nałogiem,
- 20% zgonów pośrednio zależy od palenia tytoniu,
- 10 % zgonów to związek prawdopodobny.
Palenie tytoniu to:
- 85% nowotworów płuc,
- rak pęcherza moczowego – zaprzestanie palenia nawet już po rozpoznaniu choroby nowotworowej aż 80% zmniejsza ryzyko śmierci,
- rak przełyku,
- rak trzustki.
Otyłość a choroby nowotworowe
Otyłość jest drugim – po paleniu papierosów – czynnikiem ryzyka rozwoju nowotworu złośliwego. Ma związek z następującymi nowotworami:
- rak jelita grubego,
- rak piersi u kobiet po menopauzie,
- rak trzonu macicy,
- rak nerki,
- rak przełyku,
- prawdopodobnie rak pęcherzyka żółciowego.
Zakażenia wirusowe i bakteryjne a choroby nowotworowe
Niektóre wirusy i bakterie człowieka ułatwiają występowanie nowotworów złośliwych, ich obecność lub wywołane przez nie choroby, stwarzają warunki do rozwoju raka.
Jakie bakterie i wirusy mogą być groźne?
- HPV – rak szyjki macicy, rak odbytu, rak jamy ustnej;
- HBV, HCV – rak wątroby;
- HIV – mięsak Kaposiego;
- EBV – chłoniak typu B;
- Helicobacter pylori – rak żołądka.
Z tego powodu warto wykonywać badania wykrywające obecność tych drobnoustrojów w organizmie. Wykrycie infekcji umożliwia eradykację czynnika chorobotwórczego lub wnikliwszą obserwację pacjenta i zapobiega ewentualnemu rozwojowi choroby.
Czynniki fizyczne i chemiczne występujące w środowisku
Czynniki fizyczne sprzyjające powstawaniu nowotworów to ekspozycja na światło słoneczne – rak skóry.
Czynniki chemiczne to azbest i inne czynniki środowiska pracy, na które narażeni są szczególnie pracownicy przemysłu chemicznego, hut, cementowni, fabryk farb i lakierów, itp.
Podsumowanie
Nowotwory złośliwe są przyczyną przedwczesnych zgonów bardzo wielu Polaków. Dobra informacja jest taka, iż bardzo duża część naszego zdrowia leży w naszych rękach, mamy bardzo duży wpływ na to, aby nie zachorować na nowotwór. Wystarczy aktywność fizyczna, zdrowe nawyki żywieniowe oraz badania profilaktyczne i możemy cieszyć się dobry zdrowiem do późnego wieku.
Zapraszamy do lektury II części artykułu: Rozpoznawanie nowotworów a badania laboratoryjne. Co może sugerować obecność nowotworu?
Piśmiennictwo
1. Charliński G., Jak zostać mistrzem diagnostyki hematoonkologicznej w POZ?, wykład XI Ogólnopolska Konferencja Pułapki Codziennej Praktyki Lekarskiej, online 04.09.2024-05.09.2024
2. Szczepański T., Czy zwiększoną aktywność LDH można uznać za jeden z przesiewowych parametrów u pacjentów z nawet minimalnym ryzykiem nowotworu (nieswoiste objawy)?, https://www.mp.pl/pytania/pediatria/chapter/B25.QA.11.6.1, 22.01.2015, dostęp 24.09.2024
3. Nowotwory złośliwe w Polsce w 2020 roku; Urszula Wojciechowska, Klaudia Barańska, Irmina Michałek, Paweł Olasek, Marta Miklewska, Joanna A. Didkowska; Warszawa 2022.
4. https://ecis.jrc.ec.europa.eu
5. Kobiela-Mednis A. Wybrane wskaźniki stanu zapalnego, Centrum Wiedzy ALAB laboratoria, 24 lipca 2023, https://www.alab.pl/centrum-wiedzy/wybrane-wskazniki-stanu-zapalnego/ , dostęp 24.09.2024