Choroba cywilizacyjna, jaką jest otyłość, rozwinęła potrzebę dokładniejszego poznania i zrozumienia czym jest tkanka tłuszczowa, jak funkcjonuje i jak można tę wiedzę wykorzystać w walce z otyłością. Zapraszamy do przeczytania artykułu, który syntetyzuje informacje o tym, jaką rolę tkanka tłuszczowa pełni w naszym organizmie, jakie są rodzaje tkanki tłuszczowej, co wpływa na jej powstawanie i dlaczego obecnie uważa się, że tkanka tłuszczowa jest ważną częścią układu endokrynnego.
Spis treści:
- Czym jest tkanka tłuszczowa?
- Prawidłowa zawartość tkanki tłuszczowej w organizmie
- Funkcje tkanki tłuszczowej
- Endokrynna funkcja tkanki tłuszczowej
- Rodzaje tkanki tłuszczowej
- Podsumowanie
Czym jest tkanka tłuszczowa?
Tkanka tłuszczowa jest rodzajem tkanki łącznej, składającej się z:
- adipocytów – komórek tłuszczowych,
- zrębu łącznotkankowego,
- komórek tworzących podścielisko,
- naczyń krwionośnych i limfatycznych,
- komórek układu nerwowego i immunologicznego,
- komórki macierzyste.
Dzięki takiej budowie tkanka tłuszczowa stanowi nie tylko magazyn energii, ale bierze udział w procesach metabolicznych (glikoliza, lipoliza – rozkład trójglicerydów, lipogeneza – synteza trójglicerydów, synteza białek) i jest miejscem wytwarzania licznych hormonów. Dlatego zaburzenia ilości tkanki tłuszczowej (jej nadmiar lub niedomiar) skutkują problemami w całym organizmie.
>> Przeczytaj też: Profil lipidowy – część 1: Triglicerydy
Prawidłowa zawartość tkanki tłuszczowej w organizmie
Zawartość tkanki tłuszczowej i jej rozmieszczenie w organizmie człowieka zależy od wielu czynników. Należą do nich płeć, wiek, pochodzenie etniczne, uwarunkowania genetyczne, środowiskowe i społeczne i oczywiście nawyki żywieniowe oraz aktywność fizyczna.
Najmniejszą zawartość tkanki tłuszczowej mają noworodki, stanowi ona ok. 13% ich masy ciała. Rośnie ona z wiekiem, u niemowląt (pod koniec 9. miesiąca życia) stanowi już 25-28% masy ciała, co odgrywa istotną rolę w rozwoju dziecka.
Prawidłowa zawartość tkanki tłuszczowej w wieku dorosłym u kobiet wynosi 20-30%, u mężczyzn 15-20%. Najwięcej tkanki tłuszczowej umiejscowione jest w tkance podskórnej. Za zawartość krytyczną uznaje się 33% masy ciała u kobiet i 25% u mężczyzn.
Funkcje tkanki tłuszczowej
Tkanka tłuszczowa pełni kilka funkcji w organizmie człowieka. Należą do nich:
- magazynowanie energii i zapewnienie bilansu cieplnego,
- funkcja amortyzująca,
- funkcja izolująca,
- funkcja wydzielania hormonów – endokrynna.
Podstawową funkcją tkanki tłuszczowej jest gromadzenie energii i zapewnienie prawidłowego bilansu cieplnego. Ta rola tkanki tłuszczowej staje się zrozumiała, jeśli uświadomimy sobie, że zwierzęta stałocieplne i ludzie muszą dysponować rezerwuarem energii, a tłuszcz – jako tkanka o dużej gęstości energetycznej i słabo uwodniony (w przeciwieństwie do białek czy glikogenu) – jest magazynem bardzo efektywnym.
Oblicza się, że gdyby ciało 70 kg człowieka chciało zgromadzić taką samą ilość energii w glikogenie (zawierającego dużo więcej wody), musiałoby dysponować aż 150 kg tego związku.
Poza funkcją energetyczną tłuszcz jest dobrym amortyzatorem, chroniącym narządy wewnętrzne przed urazami mechanicznymi. Spełnia również funkcję izolatora.
Bardzo ważną, stosunkowo niedawno odkrytą funkcją tkanki tłuszczowej jest jej rola endokrynna, tłuszcz wydziela bardzo wiele hormonów.
>> Przeczytaj też: Układ hormonalny człowieka. Budowa, funkcje, hormony
Endokrynna funkcja tkanki tłuszczowej
Tkanka tłuszczowa to ważny producent hormonów i innych substancji aktywnych o budowie białkowej i peptydowej. Są to hormony, adopokiny, cytokiny, i wiele innych.
Adipokiny wpływają m.in. na regulację głodu i sytości, równowagę energetyczną organizmu, działanie insuliny, biorą udział w metabolizmie glukozy i lipidów.
Adipokiny – hormony wydzielane przez tkankę tłuszczową to:
- leptyna – hormon kontrolujący uczucie głodu i sytości odgrywający bardzo ważną rolę w regulacji masy ciała i metabolizmu
- adiponektyna – białko wydzielane przez adipocyty korzystnie wpływające na metabolizm i homeostazę energetyczną całego organizmu, jej poziom często jest obniżony u osób otyłych
- rezystyna – polipeptyd, którego nazwa pochodzi od angielskiego terminu „resistence to insuline”, co oddaje jej funkcję w organizmie jako czynnika zmniejszającego wrażliwość tkanek na insulinę i rozwoju insulinooporności, wydzielana głównie przez wisceralną tkankę tłuszczową, w dużo mniejszym stopniu przez tkankę gynoidalną,
- wisfatyna,
- apelina,
- omentyna,
- iryzyna.
Cytokiny i czynniki wzrostu produkowane przez adipocyty:
- TNF-α,
- IL-6 (interleukina 6) – cytokina prozapalna odpowiedzialna m.in. za nasilanie lipolizy, wzrost oksydacji tłuszczów, endogennej glukozy oraz kortyzolu,
- IGF-1.
>> Przeczytaj też:
- Podwyższony poziom kortyzolu – objawy, przyczyny, diagnostyka, możliwości obniżenia
- Jak zbadać poziom kortyzolu? Badanie kortyzolu z krwi, śliny i moczu – różnice
Hormony:
- estrogeny – estron i estradiol – kojarzone głównie jako hormony żeńskie, jednak tkanka tłuszczowa jest ich źródłem również u płci męskiej,
- testosteron,
- hormon wzrostu.
>> Przeczytaj też: Testosteron u kobiet – co oznacza nieprawidłowy wynik?
Pozostałe związki produkowane przez tkankę tłuszczową to liczne enzymy, kwasy tłuszczowe, prostaglandyny, białka związane z układem dopełniacza i wiele innych, ocenia się, że jest ich kilkadziesiąt.
Substancje aktywne, wydzielane przez tkankę tłuszczową, wpływają na organizm człowieka na wielu różnych poziomach, zarówno w samej tkance tłuszczowej jak i w odległych tkankach i narządach. Dlatego nadmierna ilość tkanki tłuszczowej negatywne wpływa na funkcjonowanie wielu procesów metabolicznych, przyczynia się do powstawania chorób oraz rozwoju i nasilania objawów (np. cukrzycy, chorób układu sercowo-naczyniowego, PCOS, itp.)
Rodzaje tkanki tłuszczowej
Tkanka tłuszczowa u człowieka występuje pod postacią:
- białej tkanki tłuszczowej (WAT, ang. white adipose tissue)
- brunatnej tkanki tłuszczowej (BAT, ang. brown adipose tissue)
- różowej tkanki tłuszczowej (PAT, ang. pink adipose tissue)
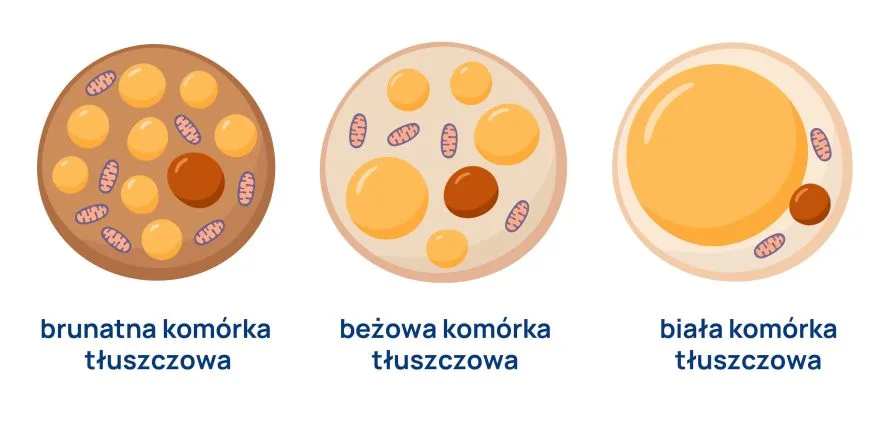
Każda z trzech postaci tkanki tłuszczowej pełni różne funkcje fizjologiczne, wspólną ich cechą jest jednak zdolność do pełnienia funkcji endokrynnych, chociaż rodzaj wydzielanych substancji i ich proporcje są różne.
Ilość tkanki tłuszczowej białej i brązowej, oraz ich wzajemne proporcje zależą do wielu czynników:
- wieku,
- metabolizmu,
- uwarunkowań środowiskowych,
- uwarunkowań genetycznych.
Badania wskazują, iż istnieją również adipocyty beżowe, powstające w wyniku transdyferencji – przemiany jednych komórek w inne, uważane za postać pośrednią pomiędzy tkanką białą i brązową.
Tkanka tłuszczowa biała (WAT)
Biała tkanka tłuszczowa jest przede wszystkim magazynem energii, gromadzonej pod postacią trójglicerydów. Większość w ten sposób przechowywanej energii pochodzi ze spożywanego pokarmu. Tkanka tłuszczowa biała charakteryzuje się dużą plastycznością – w porównaniu do innych komórek organizmu człowieka może w dużym stopniu zmieniać swój rozmiar, a tłuszcz może stanowić aż 90% objętości komórki białego adipocytu. W sytuacji nadmiernego dostarczania i gromadzenia energii prowadzi to do powstawania otyłości.
Oprócz kumulowania energii ten rodzaj tkanki tłuszczowej jest odpowiedzialny za wydzielanie wielu adipokin, dlatego ma ona poważny udział w procesach patofizjologicznych towarzyszących chorobie otyłościowej.
Tkanka tłuszczowa gromadzi się w tzw. depozytach, dla tkanki tłuszczowej białej są to depozyty:
- podskórny,
- brzuszny,
- międzynarządowy.
Rozmieszczenie białej tkanki tłuszczowej jest bardzo ważnym wskaźnikiem i czynnikiem ryzyka wystąpienia zaburzeń metabolicznych. Jeśli jej nadmiar gromadzi się w okolicy jamy brzusznej mamy do czynienia z otyłością centralną (typu jabłko), natomiast jeśli rozmieszczony jest w dolnej części ciała (biodra, pośladki) występuje otyłość gynoidalna (typu gruszka). Otyłość centralna wiąże się w ryzykiem występowanie chorób sercowo-naczyniowych, cukrzycy i innych zaburzeń metabolicznych, wisceralna tkanka tłuszczowa charakteryzuje się bowiem dużo większą aktywnością metaboliczną.

Tkanka tłuszczowa brunatna (BAT)
Ten rodzaj tkanki tłuszczowej u ssaków naczelnych i u człowieka występuje przede wszystkim we wczesnym okresie życia. U osób dorosłych zlokalizowana jest głównie w okolicach nerek i nadnerczy, na szyli i w okolicy międzyżebrowej. Jej rola polega głównie na wytwarzaniu ciepła z długołańcuchowych kwasów tłuszczowych.
Adipocyty brunatnej tkanki tłuszczowej są mniejsze niż białej, tłuszcz stanowi 30-50% ich objętości. Badania wskazują, iż długotrwała ekspozycja na zimno może aktywować BAT i zwiększać jej objętość, co obserwuje się u osób pracujących na wolnym powietrzu. Aktywacja brunatnych adopicytów do wytwarzania energii regulowana jest przez układ współczulny.
Nowsze odkrycia związane z brunatną tkanką tłuszczową pokazują, iż komórki BAT znajdują się również w białek tkance tłuszczowej i odwrotnie, co pokazuje możliwości transformacji jednych komórek w drugie.
Deficyt kaloryczny może modyfikować brunatne adipocyty, które wówczas kurczą się i zatrzymują tylko części energii wydatkowanej na termogenezę. Całkowicie skurczone adipocyty prawdopodobnie ulegają apoptozie.

Tkanka tłuszczowa różowa (PAT)
Adipocyty różowe to rodzaj komórek tłuszczowych występujących u kobiet z ciąży i karmiących. Powstają z tkanki tłuszczowej podskórnej, umiejscowione są w gruczołach piersiowych, a ich rolą jest udział w wytwarzaniu mleka.
>> Przeczytaj też: Otyłość a ciąża. Jakie są zagrożenia i konsekwencje otyłości w ciąży?
Podsumowanie
Tkanka tłuszczowa to fascynujący narząd, którego funkcjonowanie jest ciągle przedmiotem badań naukowców. To co wiemy do tej pory pokazuje jednak jak złożone procesy w nim zachodzą i dlaczego leczenie otyłości jest tak trudne.
PIŚMIENNICTWO
- Murawska-Ciałowicz E., Tkanka tłuszczowa – charakterystyka morfologiczna i biochemiczna różnych depozytów, Postepy Hig Med Dosw (online), 2017; 71: 466-484 e-ISSN 1732-2693
- Buczkowska M, Buczkowski K, Głogowska-Gruszka A, Duda S, Dyaczyński M, Nowak P. Tkanka tłuszczowa – budowa i funkcje, ze szczególnym uwzględnieniem charakterystyki wybranych adipokin i ich wpływu na organizm. Med Og Nauk Zdr. 2019;25(3):162-169. doi:10.26444/monz/110429.