Choroba Hioba, znana również jako zespół hiper IgE, to bardzo rzadki, dziedziczny niedobór odporności. W tej chorobie organizm produkuje zbyt dużo immunoglobuliny E (IgE), co skutkuje osłabioną odpornością i zwiększoną podatnością na infekcje. Dowiedz się, jakie są główne objawy tego zespołu, jak przebiega diagnostyka oraz jakie badania mogą pomóc w rozpoznaniu tego schorzenia.
Spis treści:
- Zespół hiper IgE – co to za choroba?
- Przyczyny choroby Hioba
- Zespół Hioba – jakie daje objawy?
- Diagnostyka choroby Hioba
- Leczenie choroby Hioba
- Podsumowanie
Zespół hiper IgE – co to za choroba?
Zespół hiper IgE, często nazywany chorobą Hioba, to schorzenie genetyczne, w którym układ odpornościowy nie funkcjonuje prawidłowo. Choroba ma dwie postaci – autosomalną dominującą (AD-HIES) i recesywną (AR-HIES). Najczęściej spotykana postać dominująca wynika z mutacji w genie STAT3, co prowadzi do zaburzeń w działaniu komórek odpornościowych, takich jak neutrofile i limfocyty. W efekcie osoby z zespołem hiper IgE często cierpią na nawracające infekcje bakteryjne i grzybicze, problemy skórne oraz charakterystyczne nieprawidłowości w budowie kości i zębów.
>> Przeczytaj też: Choroby rzadkie i ultrarzadkie
Przyczyny choroby Hioba
Główną przyczyną choroby Hioba jest mutacja genu STAT3, odpowiedzialnego za prawidłowe działanie komórek odpornościowych. Defekt ten powoduje, że organizm ma trudności z odpieraniem infekcji. W rzadkiej, recesywnej postaci zespołu hiper IgE przyczyny mogą leżeć w mutacjach innych genów, takich jak DOCK8 czy IL6R, które również wpływają na funkcjonowanie układu odpornościowego.
Zespół Hioba – jakie daje objawy?
Objawy zespołu hiper IgE pojawiają się najczęściej już w dzieciństwie i mogą mieć różne nasilenie. Wśród najczęstszych symptomów znajdują się:
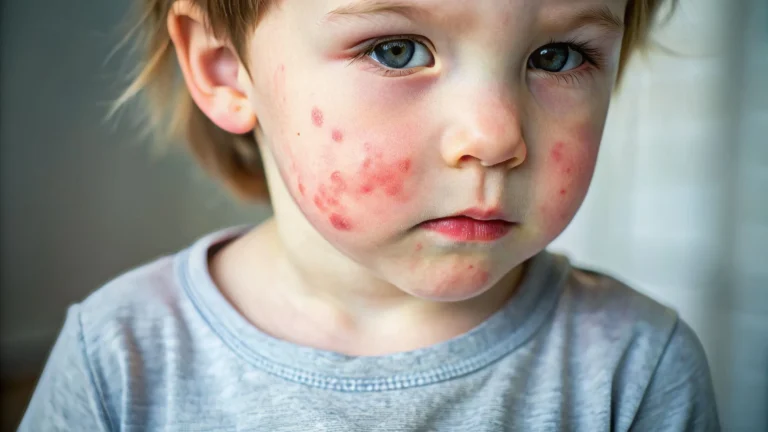
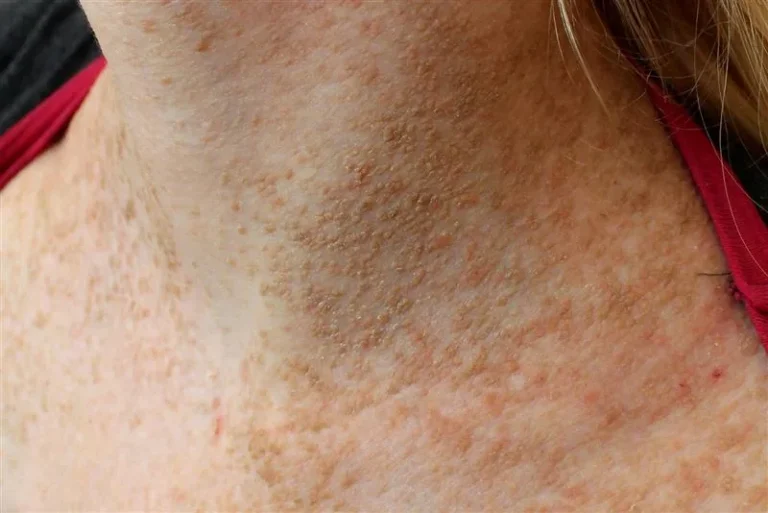
- Zmiany skórne: Częste są ropnie skórne, które bywają określane jako „zimne”, ponieważ nie wywołują typowych objawów stanu zapalnego, takich jak zaczerwienienie czy gorączka. Skóra może być również dotknięta przewlekłą egzemą oraz infekcjami grzybiczymi, np. kandydozą.
- Infekcje dróg oddechowych: Pacjenci często cierpią na nawracające zapalenia płuc, które mogą prowadzić do powstania torbieli w płucach, rozstrzeni oskrzeli i przewlekłych problemów z oddychaniem. Za infekcje te odpowiadają głównie bakterie, takie jak Staphylococcus aureus.
- Charakterystyczne rysy twarzy: U osób z zespołem hiper IgE często występują tzw. „doughy facies”, czyli miękkie, pogrubione rysy twarzy. Objawia się to szeroką nasadą nosa, wystającym czołem oraz głęboko osadzonymi oczami. Te cechy stają się bardziej widoczne z wiekiem.
- Problemy kostne i zębowe: Zespół hiper IgE może wpływać na układ kostny, prowadząc do częstych złamań kości nawet po niewielkich urazach. Często występuje również opóźnione wypadanie zębów mlecznych, co może blokować wzrost zębów stałych.
Diagnostyka choroby Hioba
Rozpoznanie zespołu hiper IgE nie jest proste, zwłaszcza że objawy mogą być podobne do innych chorób skórnych lub infekcji. Podstawą diagnostyki są:
- Badania laboratoryjne: Wysoki poziom IgE oraz eozynofilia (podwyższona liczba eozynofili) są charakterystyczne dla zespołu hiper IgE. Warto pamiętać, że wartości te mogą się różnić w zależności od osoby. Badanie poziomu IgE można wykonać, korzystając z testu Immunoglobulina IgE całkowita. Istotnym badaniem jest również morfologia krwi z różnicowaniem leukocytów, która umożliwia dokładną analizę komórek odpornościowych.
- Badania genetyczne: W przypadku podejrzenia zespołu hiper IgE przeprowadza się badania genetyczne, które mogą wykazać mutację w genie STAT3 lub innych genach odpowiedzialnych za tę chorobę. Analizę sekwencji genu STAT3 w celu potwierdzenia diagnozy można wykonać dzięki analizie genetycznej dla zespołu Hioba.
- Badania obrazowe: W razie częstych infekcji dróg oddechowych wykonuje się RTG lub tomografię klatki piersiowej, aby sprawdzić obecność torbieli płucnych lub innych zmian.


Leczenie choroby Hioba
Leczenie zespołu hiper IgE jest głównie objawowe, ponieważ obecnie nie ma skutecznej terapii przyczynowej. Najważniejsze metody leczenia to:
- Profilaktyka antybiotykowa: Ze względu na częste infekcje skórne i płucne, pacjenci z zespołem hiper IgE często przyjmują profilaktycznie antybiotyki, które zapobiegają zakażeniom wywołanym przez bakterie, takie jak Staphylococcus aureus.
- Leczenie infekcji: W przypadku wystąpienia ropni lub zapalenia płuc konieczne może być podanie antybiotyków i przeprowadzenie zabiegu drenażu. Nawracające infekcje grzybicze, takie jak kandydoza, są leczone lekami przeciwgrzybiczymi.
- Terapie immunomodulujące: W cięższych przypadkach stosuje się dożylne wlewy immunoglobulin (IVIG), które tymczasowo wzmacniają odpowiedź immunologiczną. Istnieją także eksperymentalne terapie z użyciem interferonu gamma (IFN-γ), który może wspierać walkę z infekcjami.
Współpraca z lekarzem specjalistą, takim jak immunolog lub specjalista chorób zakaźnych, jest kluczowa w leczeniu tej choroby. Dzięki odpowiedniej opiece osoby z zespołem hiper IgE mogą prowadzić relatywnie normalne życie, jednak wymagają one stałej obserwacji i częstych wizyt kontrolnych.
Podsumowanie
Choroba Hioba to rzadkie schorzenie genetyczne o wielu objawach, które mogą znacznie utrudniać codzienne funkcjonowanie. Jeśli zauważysz u siebie lub swojego dziecka objawy takie jak częste infekcje skórne, przewlekłe problemy z płucami czy trudności z zębami, warto skonsultować się z lekarzem w celu przeprowadzenia badań. Wczesne rozpoznanie i odpowiednie leczenie mogą poprawić komfort życia, chociaż choroba pozostaje trudna do całkowitego wyleczenia.
>>> Przeczytaj też: IgE całkowite – o czym świadczy wynik i w jakim celu przeprowadza się badanie?
Bibliografia
- Grzela, K. (2012). Zespół hiper-IgE (HIES) – implikacje kliniczne. Pediatria po Dyplomie, 16(4), 64-67.
- AMBOSS. „Congenital immunodeficiency disorders.” Dostępne na: https://www.amboss.com
- UptoDate. „Autosomal dominant hyperimmunoglobulin E syndrome.” Dostępne na: https://www.uptodate.com
- National Institutes of Health. Genetic and Rare Diseases Information Center (GARD). Hyper IgE syndrome;http://rarediseases.info.nih.gov/gard/10956/hyperimmunoglobulin-e-syndrome/Resources/1 (Accessed on May 27, 2014).