Artykuł został zaktualizowany 24.01.2025 r.
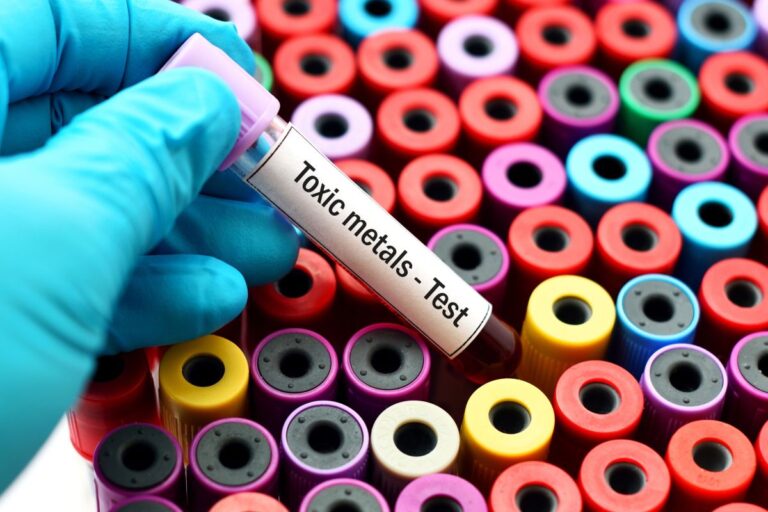
Metale ciężkie to cisi towarzysze naszego życia – nie myślimy o nich zbyt często, choć otaczają nas na każdym kroku. Tymczasem te toksyczne związki mogą wnikać do organizmu, wywierając negatywny wpływ na nasze zdrowie. Jakie mogą być objawy zatrucia metalami ciężkimi i jakie badania pozwalają je zdiagnozować?
Metale ciężkie zbędne dla procesów życiowych człowieka to między innymi kadm, rtęć i ołów. Są to pierwiastki bardzo toksyczne, których występowanie w każdym stężeniu jest niepożądane. Co więcej, poza wysoką toksycznością mają zdolność kumulacji, czyli gromadzenia się w organizmie człowieka. Stanowią one poważne zagrożenie dla zdrowia i życia, łatwo przechodzą przez łożysko i barierę krew-mózg. Mogą być przyczyną zatruć ostrych i przewlekłych. Wywołują przede wszystkim zmiany w syntezie białka i zaburzenia wytwarzania ATP, w których następstwie dochodzi do poważnych zmian chorobowych łącznie z nowotworowymi.
Metale ciężkie mogą wnikać do organizmu człowieka poprzez układ oddechowy, pokarmowy oraz przez skórę. Co ważne, skutki ich działania mogą ujawniać się dopiero po wielu latach.
Toksyczność metali ciężkich
| KADM | RTĘĆ | OŁÓW |
| Działanie rakotwórcze, uszkadza nerki, płuca i wątrobę. Powoduje choroby kostne (zaburza przemiany wapnia i fosforu), zaburzenia wzrostu i wzroku oraz bezpłodność (u mężczyzn zwykle kumuluje się w jądrach). Wypiera cynk ze ścian tętnic, prowadzi do rozwoju miażdżycy i nadciśnienia. | Silna neurotoksyna, gromadzi się w tkance mózgowej i rdzeniu kręgowym, zakłócając funkcje neurologiczne. Zaburzenie widzenia i świadomości. Stany dezorientacji i zagubienia, kłopoty z pamięcią, nerwowość, drżenie rąk. | Zatrucia przewlekłe dotyczą głównie układu pokarmowego i nerwowego. Brak apetytu, kolki, skurcze. Znużenie, zmęczenie, porażenie mięśni, osłabienie pamięci, zaburzenia neurologiczne i psychiczne. Bezpłodność oraz deformacja kości – hamuje wbudowywanie wapnia w struktury kości. Utrudnia wchłanianie jodu niezbędnego do prawidłowego funkcjonowania tarczycy. Powoduje anemię. |
Toksyczność metali ciężkich zależy od dawki, drogi narażenia, wieku, płci i stanu odżywienia narażonych osób.
Grupą szczególnego ryzyka są dzieci, u których wiele mechanizmów obronnych nie jest jeszcze aktywnych, ponieważ sam układ odpornościowy dopiero zaczyna się kształtować. Jak podaje literatura, toksyczność metali ciężkich może być jedną z podstawowych przyczyn dziecięcych zaburzeń zachowania.
>>> Przeczytaj też: Ołów – zagrożenia zdrowotne u dzieci
Kto jest narażony na nadmierny kontakt z metalami ciężkimi?
Szczególnie narażeni są pracownicy przemysłu: chemicznego, nawozów sztucznych, celulozowo-papierniczego, elektrotechnicznego, a także pracownicy rafinerii ropy naftowej, elektrowni węglowych i przemysłu koksowniczego, hutnictwa i metalurgii żelaza, przemysłu szklarskiego, ceramicznego, cementowego i azbestowego. W grupie ryzyka znajdują się również osoby zajmujące się produkcją farb, rozpuszczalników i lakierów, lamp i urządzeń pomiarowych. Jednocześnie trzeba pamiętać, że tak naprawdę każdy z nas jest narażony na toksyczne obciążenia metalami ciężkimi.
Metale ciężkie występują w zanieczyszczonym powietrzu i glebie, w wodzie z kranu, pożywieniu (warzywa, zboża, ryby, podroby zwierzęce np. wątróbka), kosmetykach chemicznych (niektóre kolorowe szminki, tusze do rzęs, cienie do powiek, podkłady, farby do włosów), plombach dentystycznych (amalgamatowych), lekach, w dymie papierosowym czy w tuszach do tatuaży.
Na każdym kroku jesteśmy narażeni na toksyczność metali ciężkich.
Statystyczna kobieta zjada kilka kg szminki w ciągu swojego życia. Wiele kolorowych szminek zawiera w swoim składzie toksyczne metale ciężkie.
Pierwiastki toksyczne mają skłonność do odkładania się w narządach miąższowych, szczególnie w wątrobie, nerkach i trzustce.
| Czy wiesz, że… Nieświadome zagrożenia kobiety w dawnych czasach używały ołowiu do wybielania cery. Aby twarz była nieskazitelna, nakładały na nią silnie toksyczną biel ołowianą zwaną cerusytem lub bielą wenecką. Ołów miał właściwości matujące i zapewniał satynowe wykończenie. Długotrwałe stosowanie powodowało przebarwienia skóry, cera stawała się szara, zmęczona, nabierała odcieni żółci, zieleni i fioletu. Ponadto ołów był również przyczyną próchnicy zębów, nieświeżego oddechu i wypadania włosów, a nawet trwałego uszkodzenia płuc. |
>>> Przeczytaj też: Grzyby i ich wartości odżywcze
Metale ciężkie występują w środowisku w ilościach takich, że niemal wszyscy jesteśmy nimi zatruci do pewnego stopnia. Jak się ich wystrzegać?
Pierwszym krokiem do podjęcia zmniejszenia ryzyka jest wykonanie badań na ich obecność. Ilościowe oznaczenie metali ciężkich we krwi pozwala w sposób pośredni zorientować się co do możliwości ich przeniknięcia przez barierę krew-mózg. Przepuszczalność tej bariery nasila się wraz ze wzrostem stężenia we krwi.
Po drugie, warto spróbować ograniczyć kontakt z metalami ciężkimi. Poniżej kilka wskazówek:
- Unikaj pokarmów wysokiego ryzyka lub je ogranicz. Należą do nich ryby słodkowodne, owoce morza, tuńczyk, mięso i podroby z intensywnej hodowli, przetworzona żywność, warzywa i owoce opryskiwane pestycydami.
- Odżywiaj się zdrowo – ważna jest zróżnicowana dieta bogata w błonnik.
- Aktywność fizyczna może wspomóc oczyszczanie.
- Odpowiedni poziom selenu, cynku, witaminy C i magnezu może pomóc przeciwdziałać toksycznym działaniom metali ciężkich. Jednocześnie pamiętaj, że więcej nie znaczy lepiej! Poziom selen i cynku również należy kontrolować, gdyż ich nadmiar jest szkodliwy.
- Stawiaj na kosmetyki naturalne.
- Usuń plomby amalgamatowe.
- Rzuć palenie! To największe źródło toksycznego kadmu.

Badanie z krwi stanowi najlepszą podstawę do oceny narażenia na metale ciężkie. Nie zwlekaj!
Pakietem pozwalającym na ocenę narażenia na najbardziej toksyczne pierwiastki w naszym otoczeniu jest PAKIET METALE CIĘŻKIE PODSTAWOWY. W pakiecie oznaczamy poziom kadmu, rtęci i ołowiu. Badania z tego pakietu wykonywane są wysoce czułą, referencyjną metodą ISP-MS, czyli spektrometrią mas sprzężoną z plazmą wzbudzaną indukcyjnie.
Materiałem do badania jest krew. Pacjent nie wymaga specjalnego przygotowania, nie trzeba być na czczo.